Por Annick BOSSU, 30 de julio de 2024
Publicado en julio de 2024 en el Reino Unido, un código deontológico contempla nuevos ámbitos de investigación en el campo biomédico: los « modelos embrionarios de células madre humanas ». Desde 2018, Francia también quiere poner límites éticos a estos embriones artificiales, conocidos como «modelos embrionarios para uso científico ». ¿Qué células madre se utilizan y con qué fin? Las consideraciones éticas esgrimidas, ¿no ocultan el deseo de desarrollar esta investigación tan codiciada?
Elaborado por investigadores de la Universidad de Cambridge (Reino Unido), el nuevo código de prácticas [1] (que no tiene valor legislativo) pretende, según sus autores, «eliminar las ambigüedades éticas y jurídicas que durante mucho tiempo han dejado a los científicos en la incertidumbre sobre los límites aceptables de su trabajo ». El tema de la reproducción en la especie humana es delicado, y los investigadores intentan disociar la investigación sobre el desarrollo de embriones humanos, por una parte, de la clínica que debe resolver los problemas encontrados durante los embarazos naturales y los fracasos de muchas fecundaciones in vitro, por otra. Sin embargo, dado que la investigación se justifica por estos problemas clínicos, la difuminación de las fronteras merece atención. Tanto más cuanto que la investigación sobre embriones humanos artificiales está en pleno auge y atrae capitales públicos y privados en numerosos países.
Muchos investigadores creen que estos modelos de embriones humanos son esenciales, porque los modelos animales han mostrado disparidades significativas con los embriones humanos. Esto se ha descubierto desde que es posible secuenciar el ARN de cada célula del embrión joven. Por otro lado, estos mismos investigadores también justifican estos modelos alternativos de embriones por la necesidad de un número cada vez mayor de ellos.
¿Cómo se obtienen estos embriones de estudio?
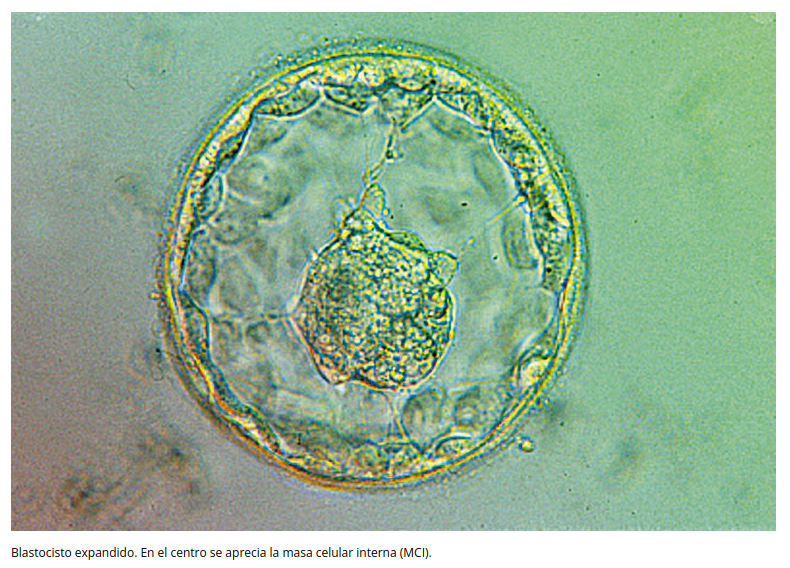
Para imitar al embrión humano es necesario disponer de modelos celulares capaces de proliferar in vitro (lo que se conoce como células madre) y con potencial para diferenciarse en todos los tipos celulares del embrión. Las células madre del embrión muy joven (blastocisto) tienen estas características. Algunas son células madre pluripotentes [3] procedentes de la parte del blastocisto que dará lugar al embrión propiamente dicho y otras son células madre que pertenecen a la parte trofoblástica del blastocisto, que dará lugar a los anexos esenciales para el desarrollo embrionario, incluida la placenta (sólo hemos podido cultivarlas desde 2020). Estos dos tipos de células madre pueden cultivarse in vitro y formar linajes [4]. Estas células se han extraído de embriones supernumerarios resultantes de la fecundación in vitro y donados a la investigación por sus padres.
Otro método para generar estas células madre consiste en reprogramar células madre somáticas (células no germinales del organismo) mediante procesos epigenéticos y genéticos: son las llamadas células madre inducidas. Se conocen como células iPS ( induced pluripotent stem) y se utilizan desde 2006. Estas células madre inducidas permiten acceder a una amplia gama de antecedentes genéticos. Utilizando estos diferentes tipos de células inducidas es posible generar los llamados modelos « integrados », es decir, que contienen todos los tipos celulares del embrión y sus apéndices.
Además, el código de conducta de los investigadores británicos establece: « el Código se aplica a todos [los modelos de embriones humanos] que contienen células humanas, sea cual sea su material de partida, incluidas las entidades que combinan material de origen humano y animal no humano». La ley francesa de bioética de 2021 también autoriza las quimeras embrionarias intraespecies y las quimeras animal-humano, es decir, las células humanas injertadas en un embrión animal, pero no a la inversa, es decir, las quimeras embrionarias humano-animal.
Cuando se cultivan in vitro en condiciones adecuadas, las células madre pluripotentes pueden ensamblarse en estructuras tridimensionales organizadas que muestran ciertas características de los embriones humanos en una fase temprana de desarrollo, de ahí el término -controvertido- de « modelo ». En muchos de estos « modelos » se observa que las distintas fases del desarrollo temprano difieren en el tiempo del embrión natural. Además, la división de estas células cultivadas in vitro no es exactamente la misma que en el embrión natural, y existen posibles mutaciones somaclonales que no están reguladas por el organismo. Por último, algunos problemas pueden desarrollarse más tarde o no manifestarse hasta más tarde.
Existe una gran variedad de estos modelos. Por ejemplo, los modelos de embriones basados en la « donación» de mitocondrias, los modelos de cíbridos, es decir, embriones humanos enucleados en los que se introduce el núcleo (material genético) de una célula somática de un organismo de otra especie o de la misma especie, los modelos de embriones de macacos en los que se ha introducido un gen humano responsable de una mayor producción neuronal (y que incluso se trasplantan a la hembra) [8]…
¿Por qué tomar precauciones éticas?
El Código de Buenas Prácticas del Reino Unido dice claramente: «Los modelos embrionarios de células madre , que se utilizan para estudiar los primeros procesos de desarrollo, tienen similitudes con los embriones humanos, pero no son embriones humanos y no están sujetos a la normativa británica que regula el uso de embriones en investigación».
En Francia, la creación de embriones por fecundación in vitro con fines de investigación está prohibida, pero la creación de estos modelos embrionarios a partir de células madre está autorizada.
Esto plantea numerosas cuestiones éticas. ¿Podrían estas estructuras desarrollarse igual que los embriones si se transplantaran in utero y, por tanto, tener un estatus moral similar al de los embriones humanos? En el caso de los modelos no integrados, sin anexos, la respuesta es claramente negativa. Sin embargo, en ratones, combinando células madre embrionarias con células madre trofoblásticas, ha sido posible obtener estructuras que imitan al embrión en estadio de blastocisto (blastoides), y que son capaces de implantarse en el útero murino. Este modelo (blastoide) se ha conseguido en la especie humana: más del 70% de las estructuras obtenidas eran similares al blastocisto desarrollado in vitro en la fase de implante (6-7 días después de la fecundación) [9]. La cuestión principal que se plantea es saber si algunos investigadores no caerán en la tentación, con fines de investigación o como medio de procreación a largo plazo, de trasplantar estos modelos en el útero cuando tengan, en su opinión, un 100% de similitud con un blastocisto natural. Se trata de una prohibición importante por el momento.
El estatus moral de un ser se determina en función de ciertas características como « ser humano “ (autoconciencia y autonomía según Kant) o ” ser sintiente ». Los bioéticos creen que un embrión no posee características que denoten racionalidad y, al menos inicialmente, tampoco sensibilidad, ya que no tiene sistema nervioso. Pero las tendrá si se le trasplanta en el útero y se desarrolla normalmente. Por tanto, las posee en potencia. El embrión es una persona humana en potencia y los modelos embrionarios también serán personas humanas en potencia si tienen el potencial de convertirse en personas. El planteamiento ético se basa, por tanto, en la representación que los bioeticistas se hacen de lo que el embrión es en sí mismo (su ontología). Sin embargo, los modelos de estudio no tienen futuro como personas, puesto que el proyecto parental ya no existe como tal. El derecho francés se basa ahora en esta característica [10].
Pero no siempre es tan sencillo. Por ejemplo, el cultivo in vitro de embriones humanos puede prolongarse ahora más allá de la fase de implantación y hasta 14 días después de la fecundación ¿Hasta dónde es aceptable llevar el desarrollo embrionario de estos modelos in vitro? ¿Es necesario recordar que actualmente se está desarrollando un útero artificial? En el extremo, ¿no tendrían algunos investigadores la tentación de aumentar el « rendimiento» de estos modelos, sabiendo que el uso de Crispr/Cas está autorizado para modificar genéticamente determinadas células madre? Por el momento, esto se limita a la corrección de genes deletéreos mediante Crispr/Cas, pero ¿será siempre así en el futuro?
En cualquier caso, poner límites a la buena conducta de los investigadores parece una señal de que el cultivo de células madre humanas puede descarriarse. De hecho, la Sociedad Internacional para la Investigación con Células Madre (ISSCR) recomendó este tipo de control en sus directrices de 2021. En el Reino Unido, por ejemplo, todo proyecto con modelos embrionarios tendrá que someterse a un comité de seguimiento formado por científicos, legisladores, sociólogos y bioeticistas. ¿Bastará con un código de buena conducta, dado que muchos de estos « expertos » trabajan en estas investigaciones?
En Francia, la Agencia de Biomedicina (ABM) es responsable de este control. La última ley de bioética (2021) ya no exige que los investigadores soliciten autorización para cultivar células embrionarias; todo lo que se requiere es una declaración de tales cultivos a la ABM. Esto plantea interrogantes sobre la fiabilidad de estos controles. Sobre todo, ¿estamos obligados a aceptar la legitimidad de estas investigaciones sometidas a controles éticos muy difíciles, si no imposibles?
[En España:
La legislación española sobre células embrionarias humanas y el desarrollo de embriones humanos artificiales se rige principalmente por la Ley 14/2007, de 3 de julio, de Investigación Biomédica. Esta ley establece el marco normativo para la investigación con células y tejidos de origen embrionario humano, así como para el uso de embriones en investigación. Los puntos clave de esta legislación son:
Prohibición de crear embriones para investigación: La ley prohíbe expresamente la constitución de preembriones y embriones humanos con fines exclusivos de experimentación.
- Autorización de técnicas de obtención de células troncales: Se permite la utilización de cualquier técnica de obtención de células troncales humanas con fines terapéuticos o de investigación, incluyendo la activación de ovocitos mediante transferencia nuclear, siempre que no implique la creación de un preembrión o embrión según la definición de la ley.
- Regulación de la investigación con muestras embrionarias: La ley establece las condiciones en las que debe llevarse a cabo la investigación con muestras biológicas de naturaleza embrionaria.
- Comisión de Garantías: Se crea la Comisión de Garantías para la Donación y Utilización de Células y Tejidos Humanos, que tiene la función de informar sobre investigaciones relacionadas con tejidos y células troncales embrionarias.
- Banco Nacional de Líneas Celulares: Se regula el Banco Nacional de Líneas Celulares, adscrito al Instituto de Salud Carlos III, para promover y coordinar la investigación con células y tejidos de origen embrionario humano.
- Control de entrada y salida de material biológico: Se requiere un informe previo favorable de la Comisión para la entrada y salida de España de gametos, preembriones,
Además, es importante mencionar que esta legislación se complementa con la Ley 14/2006, de 26 de mayo, sobre técnicas de reproducción humana asistida, que regula la donación de ovocitos y preembriones in vitro sobrantes, así como su uso en investigación. En resumen, la legislación española permite la investigación con células embrionarias humanas bajo estrictas condiciones y controles, pero prohíbe la creación de embriones humanos artificiales con fines exclusivos de experimentación.
Información obtenida mediante perplexity.ai]
Notas:
[1] Universidad de Cambridge, «Code of practice for the generation and use of human stem cell-based embryo models», julio de 2024.
[3] Pluripotente: capaz de diferenciarse en todos los tipos celulares.
[4] Mathilde Burgaud, Betty Bretin, Arnaud Reignier, John De Vos, Laurent David, «Du nouveau dans les modèles d’étude de l’embryon humain», m/s n° 2, vol. 39, febrero de 2023.
[7] Miembros del Comité de Ética del Inserm, «Research on embryos and embryonic models for scientific use (MEUS)», 2019.
[9] Mathilde Burgaud, Betty Bretin, Arnaud Reignier, John De Vos, Laurent David, «Du nouveau dans les modèles d’étude de l’embryon humain», m/s n° 2, vol. 39, febrero de 2023.
[10] Miembros del Comité de Ética del Inserm, «Research on embryos and embryonic models for scientific use (MEUS)», 2019.
—————